四、酶活性的浓度单位
50年代以前酶活性浓度单位的命名混乱,常以方法提出者的姓氏来命名,例如淀粉酶的Somogyi单位,碱性磷酸酶的King单位等等,定义参差不齐,给临床医师带来很大不便,尤其在建立“连续监测法”测酶后,大量酶应用于临床,此混乱现象更为突出。1963年国际生化协会通过广泛讨论,提出一个国际单位定义来表示酶量的多少,即1分钟能转化1微摩尔底物(μmolmin-1)的酶量为一个国际单位,以IU表示之,由于意见不一致,至今尚未指定酶反应温度,而同一量的酶,在不同温度时间为1分钟所转化底物的量将有明显差异。为避免临床上误认为只要是同一国际单位的酶量在国际上无论何处所测结果都应一致,目前大多数实验工作者常省略国际二字(简写也由IU改为U)。
临床上测定的不是酶的绝对量而是浓度,1963年并未明确规定用ml或L表示体积。旧的文献中可见到mU/ml,或U/L。目前在临床化学中,几乎都习惯用U/L来表示体液中酶活性浓度。我国由于近年来大量用自动分析仪和连续监测法测酶,已逐步不再使用各种古老单位,而使用U/L来表示酶活性浓度。
近年来国际上大力推广SI制,我国已明确SI制为法定计量单位制,SI制中酶活性单位为Katal,即1秒中转化1个摩尔底物(mol s-1)的酶量,Katal对体液中酶量而言显然过大,常用单位为ukatal或nkatal。
上述国际单位和katal间关系如下:
1U=1μmol min-1=16.67nmol s-1=16.67nkatal
在我国不论实验室还是临床医师对katal都不太熟悉,如报告使用katal/L报告酶结果时,最好同时注明相应的U/L。
(一)连续监测法中酶活性浓度的计算
前面已提到连续监测法优点之一是计算方便,不需作标准曲线或标准管,用分光光度计监测酶反应过程时,很容易求出反应体系每分钟吸光度变化,根据摩尔吸光系数可求出△A相当测定物质变化的微摩尔数,由于临床医师需要知道的是标本中而不是反应体系中酶的浓度,计算中要考虑标本的稀释倍数,假如比色杯光径不是1cm,则还应考虑光径不同对△A的影响,这样整个计算公式应为:
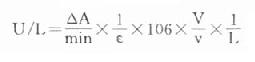
此中ε为摩尔(线性)吸光体系(mol-1·L·cm-1)
△A为吸光度变化
v为标本体积(ml)
V为反应体系体积(ml)
L为光径(cm)
在实际测定中后面几项皆为常数,所以上式常简化为:

(二)常数K的意义和设置
在测酶时,常数K值的选择是很重要的。此值过高虽然测定的线性范围较宽,但重复性差,反之,虽然精密度好,但线性窄。
此问题与仪器测定的嗓音(noise)密切相关,自动分析仪吸光度读数嗓音一般都需控制在0.001,也就是仪器须保证对同一溶液反复进行测定时,吸光度误差最好控制0.001上下,虽然此值不大,但已可能使测定结果产生1/1000K值的误差,如K值为6000,代入上式,则每分钟测定吸光度如有0.001微小变化,结果将是出现上下6U/L的误差,对于一此参考值较低的酶,如转氨酶而言显然太大,临床医师无法容忍这么大差异。
K值设置的首先出发点应是测定酶的判断值或参考值上限,应保证这些值测定的可靠,所以转氨酶的常数K一般在3000左右,不少人宁愿在1500左右,另外还应考虑到测定时间,一些半自动分析仪测定时间短到0.5分,此时0.001嗓音对每分钟△A误差将是0.002,反之,测定时间延长到2分钟,误差也小一半,也就是说,如测定时间长,则K值可以设置大一些,如测定时间只有0.5分钟,K值一般不超过4000。
改变K值最方便的途径就是改变标本稀释度,稀释倍数愈大,K值愈大。
(三)常数K值的检验
摩尔吸光系数(ε)对一定物质而言常是一个定值,但在一些外界条件影响下也会有所变化。最明显例子是对硝基酚,随pH不同,颜色差异明显,当pH>10时,405nm处其ε为18500,在pH7.0,ε下降为9400,颜色下降几乎一半。温度变化时,也会对NAD(P)H的ε产生一些影响。当波长大于334nm时,随温度升高,同一波长的ε值会轻度下降。
同时ε值是指用分光光度法,也就是在近似单色光的光源条件下才能成立,实际上大多数自动分析仪使用的是干涉滤片,波峰值可能出现差异,个别的半波宽可能为10nm乃至更大。由于杂散光的存在,会明显改变ε值,假如再考虑到注加系统的误差,实测K值很可能与理论K值不一致。Onuki检测了三台Hitachi-7150型自动分析仪测AST的K值分别为-5466、-5421、-5559。而理论K值为-6111则结果约增加为1.12倍。
测定实际的K值不是一件困难的事,目前有些自动分析仪已有相应的软件和试剂可以进行检测。事实上对一些性质稳定的物质如对硝基酚、对硝基苯胺,可以用高纯试剂配成标准品或直接购买可靠的校准品,将它们作为标本进行酶的测定,根据已知标准品的浓度和吸光度变化就可计算出实际K值,但此法不适用于测与NAD(P)H反应有关酶测定的K值。因为NAD(P)H不稳定,此时可使用测葡萄糖的紫外分光光度法试剂盒,对已知浓度的葡萄糖标准品进行终点法测定,此法产生与葡萄糖相等摩尔数的NAD(P)H,故不难从吸光度变化求出K值,也有人用乳酸脱氢酶测已知量的丙酮酸来求K值。

- 酶活性的浓度单位《临床生物化学》
- 酶活性测定条件的选择和限定《临床生物化学》
- 酶活性降低引起的遗传性酶病《医学遗传学基础》
- 酶活性测定的常用技术和方法《临床生物化学》
- 酶活性增高引起的遗传性酶病《医学遗传学基础》
- 酶活力测定《临床生物化学》
- 酶扩大免疫测定技术《免疫学和免疫学检验》
- 酶含量调节《生物化学与分子生物学》
- 酶类标志物《临床生物化学》
- 酶分子降解的调节《生物化学与分子生物学》
- 酶免疫测定的应用《免疫学和免疫学检验》
- 酶分子化学修饰调节《生物化学与分子生物学》
- 酶免疫技术的分类《免疫学和免疫学检验》
- 酶法(GK-GPO-POD比色法)《动脉粥样硬化》
- 酶免疫技术的分类《免疫学和免疫学检验》
- 酶法(CEH、COD-POD法)《动脉粥样硬化》
- 酶浓度对反应速度的影响《生物化学与分子生物学》
- 酶法《动脉粥样硬化》
- 酶桥法《实用免疫细胞与核酸》
- 酶法《动脉粥样硬化》
- 酶系统《病理学》
- 酶的作用特点《生物化学与分子生物学》
- 酶消化液《实用免疫细胞与核酸》
- 酶的种类及特点《实用免疫细胞与核酸》
- 酶原《生物化学与分子生物学》
- 酶的命名《生物化学与分子生物学》
- 酶作用高效率的机理《生物化学与分子生物学》
- 酶的分子组成《生物化学与分子生物学》
- 酶作用在于降低反应活化能《生物化学与分子生物学》
- 酶的分子结构和活性中心《生物化学与分子生物学》
- 霉变甘蔗中毒《家庭医学百科-自救互救篇》
《临床生物化学》
- 第一章 绪论
- 第二章 蛋白质与临床诊断
- 第一节 健康与疾病时的血浆蛋白质
- 第二节 细胞骨架蛋白——组织特异性蛋白的鉴定及其意义
- 第三节 细胞调节因子
- 第三章 糖代谢紊乱
- 第四章 血浆蛋白及其代谢紊乱
- 第五章 体液平衡紊乱
- 第一节 体液平衡及调节
- 第二节 血气分析
- 第三节 体液平衡紊乱
- 第四节 酸碱平衡紊乱
- 第五节 酸碱平衡紊乱典型病例检验结果分析
- 第六节 体液钾钠氯测定及方法学评价
- 第六章 钙磷镁与微量元素的临床生物化学
- 第一节 钙、磷代谢及其异常
- 第二节 镁代谢及其异常
- 第三节 微量元素的作用及其与疾病的关系
- 第七章 诊断酶学
- 第一节 概述
- 第二节 临床诊断中常用的血清酶类及其同工酶
- 一、肌酸激酶(CK)及其同工酶
- 二、乳酸脱氢酶(LD)及其同工酶
- 三、氨基转移酶(ALT,AST)及其同工酶
- 四、碱性磷酸酶(ALP)
- 五、γ-谷氨酰基转移酶及其同工酶
- 六、淀粉酶(AMY)及其同工酶
- 七、酸性磷酸酶(ACP)及其同工酶
- 第三节 缺血性冠状动脉疾病的酶学诊断
- 第四节 肝脏疾病的酶学诊断
- 第八章 肿瘤标志物的临床实验室检查
- 第九章 治疗药物监测
- 第一节 概论
- 第二节 药代动力学基础及有关参数的应用
- 第三节 合理使用治疗药物监测应考虑的基本因素
- 第四节 治疗药物监测的临床应用
- 第五节 治疗药物监测常用标本及预处理
- 第六节 药物浓度测定常用技术
- 第七节 需测定药物浓度进行监测的主要药物
- 第十章 肝胆疾病的生物化学与实验诊断
- 第一节 概述
- 第二节 肝的生物转化功能
- 第三节 肝与胆汁酸代谢
- 第四节 胆红素代谢与黄疸
- 第五节 某些肝病的生化机制
- 第六节 肝细胞损伤时的肝功能试验
- 第十一章 肾功能不全的实验室生物化学诊断
- 第一节 概述
- 第二节 常见肾脏疾病的病理生物化学
- 第三节 肾功能不全的生化诊断及评价
- 第十二章 内分泌疾病的生物化学诊断
- 第一节 概述
- 第二节 甲状腺功能紊乱的临床生化
- 第三节 肾上腺功能紊乱的临床生化
- 第四节 下丘脑-垂体内分泌功能紊乱的临床生化
- 第五节 性激素紊乱的临床生化
- 第十三章 神经、精神疾病的生物化学
- 第一节 概述
- 第二节 某些神经疾病的生物化学
- 第三节 精神性疾病的生物化学
- 第四节 神经、精神疾病生化诊断
- 第十四章 妊娠的临床生物化学
- 第十五章 遗传性疾病的生物化学与分子生物学诊断
- 第十六章 常用分析技术在临床生物化学中的应用
- 第一节 光谱分析技术的应用
- 第二节 电泳技术的应用
- 第三节 离心技术的应用
- 第四节 层析技术的应用
- 第五节 电化学分析技术的应用
- 第十七章 血清酶定量的检测技术
- 第一节 概述
- 第二节 酶活性测定的常用技术和方法
- 第三节 酶活性测定条件的选择和限定
- 第四节 测定酶活性浓度的两大类方法
- 第十八章 诊断分子生物学基本技术
- 第一节 概述
- 第二节 分子生物学实验基础
- 第三节 分子生物学实验诊断技术
- 第四节 诊断分子生物学技术的临床应用
- 第十九章 临床生物化学分析仪的性能与应用
- 第一节 临床生化自动分析仪的类型
- 第二节 临床生化自动分析仪的性能评价与合理选用
- 第三节 临床生化自动分析的方法
- 第二十章 临床生物化学方法的选择、建立和评价
- 第一节 临床生化方法的选择
- 第二节 临床生化方法的建立
- 第三节 临床生化方法学的评价
- 第四节 临床生化方法学性能判断
- 第二十一章 临床生物化学检验质量控制
- 第二十二章 临床生物化学实验室数据的作用和有效使用











