一、酶的分子组成
根据酶的组成成份,可分单纯酶和结合酶两类。
单纯酶(simpleenzyme)是基本组成单位仅为氨基酸的一类酶。它的催化活性仅仅决定于它的蛋白质结构。脲酶、消化道蛋白酶、淀粉酶、酯酶、核糖核酸酶等均属此列。
结合酶(conjugatedenzyme)的催化活性,除蛋白质部分(酶蛋白apoenzyme)外,还需要非蛋白质的物质,即所谓酶的辅助因子(cofactors),两者结合成的复合物称作全酶(holoenzyme),即:
| 全酶 | =酶 蛋 白 | + 辅助因子 |
| (结合蛋白质) | (蛋白质部分) | (非蛋白质部分) |
酶的辅助因子可以是金属离子,也可以是小分子有机化合物。常见酶含有的金属离子有K+、Na+、Mg2+、Cu2+、(或Cu+)、Zn2+和Fe2+(或Fe3+)等。它们或者是酶活性的组成部分;或者是连接底物和酶分子的桥梁;或者在稳定酶蛋白分子构象方面所必需。小分子有机化合物是些化学稳定的小分子物质,其主要作用是在反应中传递电子、质子或一些基团,常可按其与酶蛋白结合的紧密程度不同分成辅酶和辅基两大类。辅酶(coenzyme)与酶蛋白结合疏松,可以用透析或超滤方法除去;辅基(prostheticgroup)与酶蛋白结合紧密,不易用透析或超滤方法除去,辅酶和辅基的差别仅仅是它们与酶蛋白结合的牢固程度不同,而无严格的界限。
现知大多数维生素(特别是B族维生素)是组成许多酶的辅酶或辅基的成分(见表2-1)。它们的化学结构式见生物氧化章。体内酶的种类很多,而辅酶(基)的种类却较少,通常一种酶蛋白只能与一种辅酶结合,成为一种特异的酶,但一种辅酶往往能与不同的酶蛋白结合构成许多种特异性酶。酶蛋白在酶促反应中主要起识别底物的作用,酶促反应的特异性、高效率以及酶对一些理化因素的不稳定性均决定于酶蛋白部分。
表2-1 B族维生素及其辅酶形式
| B族维生素 | 辅酶形式 | 主要作用 |
| 硫胺素(B1) | 硫胺素焦磷酸酯(TPP) | α-酮酸氧化脱羧酮基转换作用 |
| 硫辛酸 | 6,8-二硫辛酸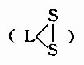 | α-酮酸氧化脱羧 |
| 泛酸 | 辅酶A(CoA) | 酰基转换作用 |
| 核黄素(B2) | 黄素单核苷酸(FMN) 黄素腺嘌呤二核苷酸(FAD) | 氢原子转移 氢原子转移 |
| 尼克酰胺(PP) | 尼克酰胺腺嘌呤二核苷酸(NAD+) 尼克酰胺腺嘌呤二核苷酸磷酸(NADP+) | 氢原子转移 氢原子转移 |
| 吡哆素(B6) | 磷酸吡哆醛 | 氨基酸代谢 |
| 生物素(H) | 生物素 | 羧化作用 |
| 叶酸 | 四氢叶酸 | “一碳基团”转移 |
| 钴胺素(B12) | 5-甲基钴铵素 5-脱氧腺苷钴铵素 | 甲基转移 |

- 酶的分子组成《生物化学与分子生物学》
- 酶的分子结构和活性中心《生物化学与分子生物学》
- 酶的命名《生物化学与分子生物学》
- 酶的分类《生物化学与分子生物学》
- 酶的种类及特点《实用免疫细胞与核酸》
- 酶蛋白合成的诱导和阻遏《生物化学与分子生物学》
- 酶的作用特点《生物化学与分子生物学》
- 酶促反应的动力学《生物化学与分子生物学》
- 酶法《动脉粥样硬化》
- 酶标抗体的纯化《实用免疫细胞与核酸》
- 酶法《动脉粥样硬化》
- 酶《生物化学与分子生物学》
- 酶法(CEH、COD-POD法)《动脉粥样硬化》
- 煤炭《本草分经》
- 酶法(GK-GPO-POD比色法)《动脉粥样硬化》
- 煤气中毒的急救《现代院外急救手册》
- 酶分子化学修饰调节《生物化学与分子生物学》
- 煤毒熏晕《奇效简便良方》
- 酶分子降解的调节《生物化学与分子生物学》
- 煤《本草撮要》
- 酶含量调节《生物化学与分子生物学》
- 腜(mei媒)《中医词典》
- 酶活力测定《临床生物化学》
- 媒介节肢动物传播《预防医学》
- 酶活性测定的常用技术和方法《临床生物化学》
- 脢《中医词典》
- 酶活性测定条件的选择和限定《临床生物化学》
- 梅子丸《饮膳正要》
- 酶活性的浓度单位《临床生物化学》
- 梅子《饮食须知》
- 酶活性降低引起的遗传性酶病《医学遗传学基础》




