(四)染色原理及步骤
1.基本原理酶标抗体与荧光色素标记抗体的染色相同,亦分直接法和间接法。直接法是将酶直接标记在每一抗体上,间接法是将酶标记在第二抗体上,检测组织细胞内的特定抗原物质。间接法所用的第一抗体是对组织细胞内某种抗原的特异性抗体(80%~90%的抗血清系由家兔制得,而绝大数单克隆抗体系由小鼠制备);第二抗体则为第一抗体(家兔/小鼠的IgG)的抗体。所以,只要不同的第一抗体均来自同一种属,同一标记的第二抗体就能用来显示其不同特异性抗原的存在,这样可避免了直接法中标记每一种第一抗体的麻烦,并且提高了方法的敏感度。目前的ICC染色中,以间接法为常用,在此着重介绍间接法的染色程序。
2.染色程序
(1)切片准备:见第一章 。
①石蜡切片经二甲苯或Hemo-De脱蜡,下行酒精至水。②固定/无固定新鲜组织冰冻切片,室温干燥2h以上。
(2)未固定的新鲜组织切片,丙酮固定20~30min(fretrieval ),简而言之,即用蛋白酶处理,去除固定剂交联造成的空间遮蔽(室温),风干15~30min.;已固定的组织冰冻切片及石蜡切片,根据需要可进行组织抗原的激活。
(3)用蜡笔沿切片周围勾划一道屏障,以避免孵育液流失及孵育过程中切片干燥,同时也能节 省抗体用量,保持切片与抗体的充分接触,风干。石蜡切片(滴少量PBS,以防其干燥)直接进行步骤(6)。
(4)切片经PBS或其它缓冲液漂洗3次,每次2min,溶解除去冰冻切片上的OCT包埋剂。但应用ALP标记抗体时,禁用二甲胂酸钠缓冲液漂洗,因后者可使ALP失活。
(5)根据需要,用甲醇+0.3%H2O2处理切片15~30min(室温),封闭内源性过氧化酶的活性。应用ALP标记抗体时,此步可省略。
(6)PBS漂洗2min(共两次),移至0.05%Tween-20/PBS(或0.22~1%Triton X-100)中5min(室温)。Tween-20为一种表面活性剂,除具有清洁作用外,还可增加组织的通透性,有利于组织细胞内抗原的显示。
(7)4%BlockAce或0.1%~1%BSA湿盒内孵育15~25min(室温),然后;轻轻弃去孵育液(不冲洗);以阻断组织与抗体的非特异性结合,降低背景染色。
(8)根据需要,可用1/5~1/30正常来活兔/羊血清孵育15~20min(室温,以酶标抗体相同种属正常血清为宜,最好是同一动物免疫前的血清)。或者省略此步,而在稀释酶标抗体时,加入1%~2%的同一种属正常血清。
(9)轻轻弃去孵育液, 滴加含0.2%BSA/0.05 NaN3/PBS稀释的第一抗体(抗体用量:每张切片一般为50~80μl),湿盒内孵育1~2h(20~25℃);免疫电镜用标本,4℃过夜。
(10)PBS充分冲洗(3次×2min),以去除切片上非特异吸附的抗体。应用不同的第一抗体或同时进行对照标本染色时,需分别冲洗,以防相互污染。
(11)经0.05%Tween-20/PBs2min后,滴加含0.2%BSA/1%正常血清/PBS稀释的HRP酶标记的第二抗体,湿盒内孵育45~60min(20~25℃)。
(12)PBS漂洗(3次×2min),此处不需分别漂洗,因所有切片均系同一酶标抗体孵育。
(13)未固定或固定较弱的冰冻切片,此处可轻微固定。首先将切片从PBS移至TBS中3~5min,去除PBS,以防其中的磷酸与后面使用的固定液中的CaCl2形成磷酸钙而沉淀后,然后用Baker氏固定液固定5min(室温)此时轻微固定,既不影响抗原抗体结合,又较有利于保存第一抗体孵育前的组织抗原,尤其适用于单克隆抗体的ICC染色。
(14)呈色:HRP标记抗体的呈色液为0.01%~0.1%H2O2 0.01%~0.05% DAB 0.05~0.1mol/L Tris –HCl(pH7.4)。切片经PBS或Tris-HCl液漂洗后,置上述呈色液内10~15min(室温、暗处),亦可镜下控制显色速度。终产物为棕褐色沉淀。用于电镜观察的标本,呈色3~5min即可,防止DAB终产物向周围扩散,影响超微结构定位。另外,显色液应于用前新鲜配制,避免DAB本身氧化变质。新配制的DAB为无色透明液体。若DAB液已氧化变为紫红色,应换新药重新配制。
(15)将切片置流水中(仅光镜观察)或PBS(电镜标本)内,终止呈色反应。
(16)未固定的冰冻切片,可用1%戊二醛-PBS液加强固定5~10min(室温),流水冲洗。
(17)细胞核轻度染色,以甲基绿和苏木精为常用。前者细胞核呈绿色,与HRP/ALP等终产物对比度尤佳,但不适于微波照射的标本。苏木精是组织学、病理学研究中普遍应用的核染色方法,与HRP、ALP的终产物对比度比较好。
(18)DAB呈色的标本,可以系列酒精脱水、Hemo-De透明、DPX封固。其它物质呈色的标本,在有机溶剂中沉淀物易溶解,褪色,所以用水溶性封固剂如明胶甘油等封固,次日,于盖玻片周围涂少许女士用指甲油,可使切片保存时间更长。
(19)镜检、观察记录同一般形态学研究。
(20)免疫电镜用标本,经OSO4后固定,按电镜标本要求处理(参见本书第七章 )。亦可OSO4固定,喷碳(Carbon Coating),利用扫描电镜观察抗原的存在部位。
3.酶标抗体及发色剂的选择

HRP特异底物为H2O2,在分解H2O2过程中,与H2O2形成复合物,无电子供体存在时,反应不再进行,当电子供体存在时,迅速生成水,酶被还原,电子供体被氧化环化,形成苯乙胼聚合体(图4-2)。在酶反应部位,形成不溶性棕褐色沉淀,与组织对比清晰。
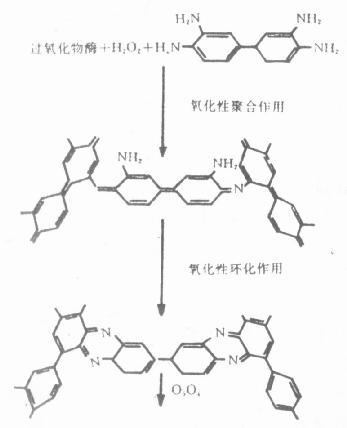
图4-2 DAB反应产物形成过程
HRP催化的酶促反应第一步是特异性的—酶催化底物H2O2,其余反应是非特异的,可用各种电子供体介导,所以选用不同的电子供体,可使终产物呈不同颜色,例如:CN(4—Chloro—1– N aphthol)为蓝黑色,TMB(Tetramethyl—Benzidine )为深蓝色,AEC(3—amino—9– ethyl--carbazole)为红色。市售试剂盒所配显色液以AEC居多,室温下较稳定,但不能进行脱水等处理,且时间长易褪色。DAB是广泛应用的电子供体之一,较敏感,切片可脱水透明、半永久保存,且终产物具有嗜饿性,经O2O4处理,电子密度增加,适于电镜下确定抗原的存在部位。但是DAB被认为可能具有致癌性,所以应尽量减少吸入和接触次数,最好将DAB制成10倍贮存液,分装于-20℃保存,应用时稀释、过滤。与DAB比较,CN敏感性略差,但因其终产物较局限,很少弥散,光镜观察较为适合。
(2)ALP,是以As-Mx为底物,FB/FR为发色团,生成蓝色/红色不溶性沉淀。ALP标记抗体主要用于内源性过氧化酶含量较高的血细胞、淋巴细胞等的ICC染色。显色液内加入终浓度为2~4mmol/l的levamisole, 大多数内源性ALP活性可被抑制。通常左旋咪唑(levamisole)以每毫升60~120mmol/L浓度的贮存液-20℃冰箱保存。应用时稀释30倍。为避免反复称取,试剂吸水,As-Mx、FR、FB试剂均应小量分装后-20℃冰箱保存,左旋咪唑能抑制内源性碱性磷酸酶活性。例如:以每次所用显色液30ml计算,分装As-Mx 5~7mg/支、Fr8mg./支、FB7mg/支,每次使用一支,用前稀释30倍,过滤显色。FR、FB等在光照射条件下易引起沉淀,故显色反应在暗处进行。
(3)GOD,是以葡萄糖为底物的酶,其显色方法为β-D-葡萄糖67mg、NBT6.7mg、PMS(Phenazine Methylsulfate)0.167mg,0.05mol/L PB(pH8.3)10.0ml,37℃孵育1h。生成蓝色不溶性沉淀。该终产物不溶于有机溶剂,切片可脱水透明,长期保存。但GOD的敏感度较HRP和ALP为低,电子供体少,应用较局限,主要用于两种酶的放大技术,能提高方法和敏感性和特异性。即用GOD和HRP分别标记第二、第三抗体(例第一抗体为小鼠单克隆抗体、第二抗体为GOD标记的兔抗鼠IgG,第三抗体则为HRP标记的羊抗兔IgG),ICC染色,以葡萄糖-DAB作显色剂。基本原理如(图4-3)。在这里HRP是作为第二酶系统,利用葡萄糖氧化时生成的H2O2作底物,催化酶促反应,不受内源性过氧化酶的影响。而且GOD和HRP所标记的抗体是结合在同一抗原位置,所以能良好地显示组织抗原的存在。其主要染色步骤为:
①切片经第一抗的孵育;②漂洗,GOD标记的第二抗体孵育40~60min(室温);③漂洗,HRP标记的第三抗体孵育30~45min(室温);④漂洗,显色、脱水透明观察同前。
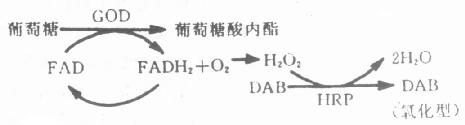
图4-3 两步酶催化反应原理

- 染色原理及步骤《实用免疫细胞与核酸》
- 染色体异常发生的频率《医学遗传学基础》
- 染色质和核小体《生物化学与分子生物学》
- 染色体异常《默克家庭诊疗手册》
- 染苔《中医名词词典》
- 染色体畸变综合征的概念。《医学遗传学基础》
- 染苔《中医词典》
- 染色体畸变综合征《医学遗传学基础》
- 染症《万氏秘传片玉心书》
- 染色体畸变《核、化学武器损伤》
- 瀼泄《中医词典》
- 染色体的形态结构《实用免疫细胞与核酸》
- 禳久病不愈,一切怪症奇疮善法小神作祟亦同《医理真传》
- 染色体的数目畸变《医学遗传学基础》
- 禳疟法《备急千金要方》
- 染色体的结构异常《医学遗传学基础》
- 禳疟法六首《外台秘要》
- 染色体错误配对不等交换《医学遗传学基础》
- 禳谢法《幼幼新书》
- 染色体不稳定综合征《医学遗传学基础》
- 禳厌法《证治准绳·幼科》
- 染色体病《病理学》
- 让实《千金翼方》
- 染色体G显带技术《实用免疫细胞与核酸》
- 让实《新修本草》
- 染色特异性和敏感性的测定《实用免疫细胞与核酸》
- 让实《证类本草》
- 染色技术的选择性《实用免疫细胞与核酸》
- 让实《名医别录》
- 染色《实用免疫细胞与核酸》
- 荛(音饶)花《证类本草》




